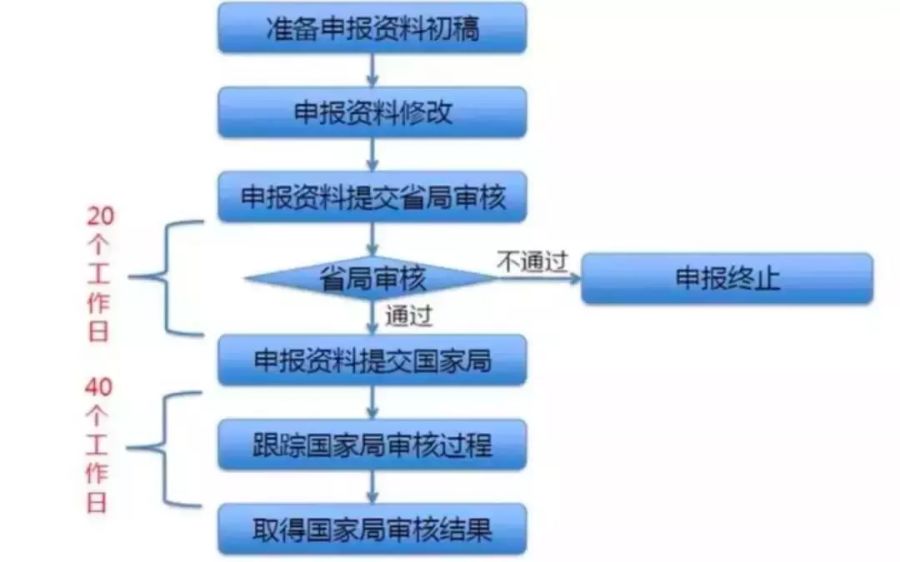
對于醫(yī)療器械生產初創(chuàng)企業(yè)而言�����,產品從研發(fā)設計階段到走向消費市場����,至少應經歷設計開發(fā)����、注冊檢測、臨床試驗�����、注冊申報���、生產許可申請等漫長的無盈利過程���。那么����,如何評估產品安全性風險��、申報注冊周期��、投入資金與成本���?都是初創(chuàng)企業(yè)創(chuàng)始人最關心的問題�����?����;谏鲜鰡栴},小編進行按照醫(yī)療器械產品設計開發(fā)�、體系建立、創(chuàng)新產品申報(若涉及)����、注冊檢測�、臨床試驗�、注冊申報、生產許可申請��、產品上市等必要階段進行簡單整理�����。
產品設計開發(fā)流程
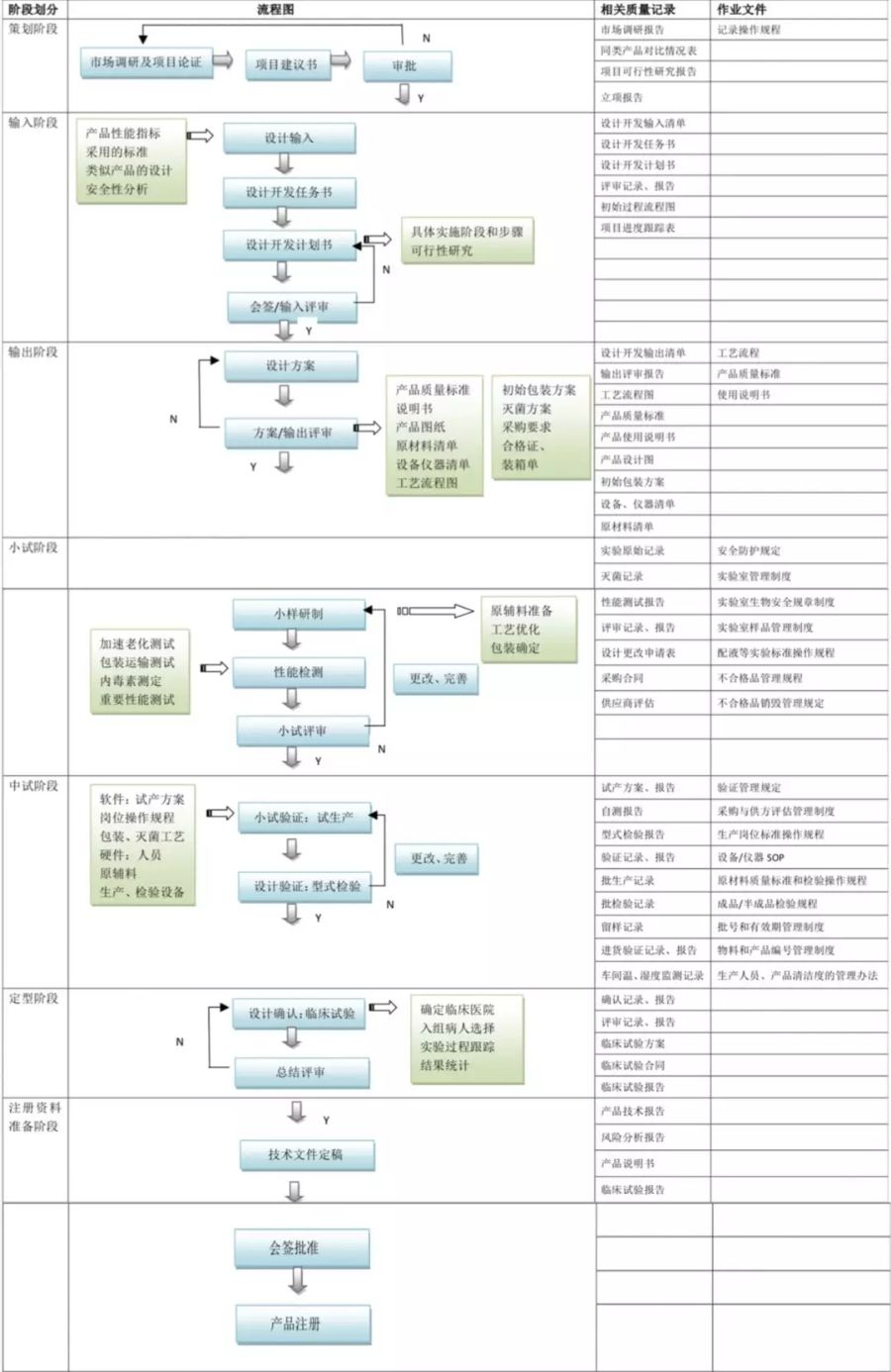
產品設計開發(fā)可分7個階段:策劃階段���、設計輸入階段����、設計輸出階段�、小試階段、中試階段�、定型階段、注冊資料準備階段���。
產品設計開發(fā)要點
一般而言�����,創(chuàng)始人創(chuàng)立公司是基于科研成果與產品布局基礎上�,并已初步具備研發(fā)團隊、合作伙伴等���。但無論如何���,對于初創(chuàng)公司而言,因涉及大量資金注入與技術攻堅�,產品設計開發(fā)階段十分艱難,時間也是難以預估的��,短則數(shù)月����,長則數(shù)年。那么����,如何在產品設計開發(fā)階段降低成本,滿足需求���,增加創(chuàng)新?
首先���,產品技術層面�����,專業(yè)高效的研發(fā)團隊是前提和基礎���;其次���,法規(guī)層面建議尋找專業(yè)研發(fā)服務公司或引進法規(guī)團隊對產品開發(fā)進行嚴格的風險評估,明確產品申報類型等����。但我們常常發(fā)現(xiàn),很多新辦企業(yè)在產品已定型�����、開模后���,才開始引進法規(guī)人員或尋找咨詢機構���。此時的建議和措施往往基于補救,嚴重的可能涉及改模���、重新設計等���。所以對于新辦企業(yè)而言�,法規(guī)前置應慎重考量����。最后,還應關注產品專利布局����。公司應重點布局核心技術的知識產權保護;同時�,考慮核心技術轉讓、購買等問題��。產品的專利申報可以委托相應機構����,后期若涉及專利較多,亦可引入專職人員���。
創(chuàng)新醫(yī)療器械申報
2014年2月7日����,原國家食藥監(jiān)總局發(fā)布了《創(chuàng)新醫(yī)療器械特別審批程序(試行)》(食藥監(jiān)械管〔2014〕13號),此文件自2014年3月1日起施行�。該程序是在確保上市產品安全�����、有效的前提下�,針對創(chuàng)新醫(yī)療器械設置的審批通道,但也有嚴苛的審批標準:
(1)產品核心技術發(fā)明專利權,審批申請人經過其技術創(chuàng)新活動����,在中國依法擁有產品核心技術發(fā)明專利權,或者依法通過受讓取得在中國發(fā)明專利權或其使用權,或者核心技術發(fā)明專利的申請已由國務院專利行政部門公開;
(2)國內首創(chuàng)產品,主要工作原理/作用機理為國內首創(chuàng)�����,產品性能或者安全性與同類產品比較有根本性改進���,技術上處于國際領先水平�����,并且具有顯著的臨床應用價值;
(3)產品基本定型,申請人已完成產品的前期研究并具有基本定型產品�����,研究過程真實和受控��,研究數(shù)據(jù)完整和可溯源���。
若企業(yè)醫(yī)療產品設計滿足上述要求��,則應著手申報創(chuàng)新���。創(chuàng)新特別審批是申請人已完成產品的前期動物研究并具有基本定型產品即可申報。